-
FDA受理流感药Xofluza用于流感并发症高危人群补充新药申请
瑞士制药企业罗氏近日宣布,美国食品和药物管理局(FDA)已受理Xofluza(baloxavir marboxil)的补充新药申请(sNDA),作为一种单剂量、口服药物,用于流感并发症高危人群。美国疾病控制和预防中心(CDC)将严重流感并发症的高危人群定义为:65岁及以上老年人群,或患有哮喘、慢性肺病、病态肥胖或心脏病等疾病的人群。FDA预计将在2019年11月4日之前做出最终审查决定。罗氏首席医疗官兼全球产品开发主管Sandra Horning表示,“流感对于高危人群来说,尤其会使其虚弱,因为
2019-03-08 -

艾伯维潜在重磅产品Skyrizi获欧盟CHMP支持批准,治疗斑块型银屑病
美国生物技术巨头艾伯维(AbbVie)近日宣布,欧洲药品管理局(EMA)人用医药产品委员会(CHMP)已发布积极审查意见,推荐批准Skyrizi(risankizumab)用于适合系统治疗的中度至重度斑块型银屑病成人患者。用药方面,Skyrizi在第0、4周分别用药一次,之后每3个月(12周)用药一次,剂量为150mg(2针75mg),皮下注射。CHMP的建议将递交至欧盟委员会(EC),EC在做出最终审查决定时通常都会采纳CHMP的意见。这也意味着,Skyrizi极有可能在未来2-3个月获批,造
2019-03-04 -
第3代肺癌靶向药!辉瑞ALK抑制剂Lorviqua在欧盟即将获批,治疗ALK阳性肺癌
美国制药巨头辉瑞(Pfizer)近日宣布,欧洲药品管理局(EMA)人用医药产品委员会(CHMP)已发布积极审查意见,推荐有条件批准Lorviqua(lorlatinib),作为一种单药疗法,用于接受alectinib(艾乐替尼)或ceritinib(色瑞替尼)作为首个ALK-TKI疗法、或接受crizotinib(克唑替尼)及至少一种其他ALK-TKI治疗后病情进展的ALK阳性晚期非小细胞肺癌(NSCLC)成人患者Lorviqua由加速批准转为正式批准将取决于证实积极效益-风险平衡的综合数据集。
2019-03-04 -
赛诺菲/再生元Dupixent哮喘新适应症获批在即
法国制药巨头赛诺菲(Sanofi)与合作伙伴再生元(Regeneron)近日联合宣布,欧洲药品管理局(EMA)人用医药产品委员会(CHMP)已发布积极意见,推荐批准Dupixent(dupilumab)作为一种附加维持疗法,用于接受高剂量吸入性皮质类固醇联合另一种药物用于维持治疗但病情控制不佳的2型炎症重度哮喘的青少年(12岁及以上)和成人患者,2型炎症特征为血液嗜酸性粒细胞增多和/或呼出气一氧化氮(FeNO)升高。现在,CHMP的意见将递交至欧盟委员会(EC)审查,并将在未来2-3个月内作出审
2019-03-04 -

首个!Amicus庞培病疗法获突破性疗法认定
日前,Amicus Therapeutics公司宣布,美国FDA授予其在研疗法AT-GAA突破性疗法认定,用于治疗晚发型庞培病(Pompe disease)。庞培病是由于酸性α-葡萄糖苷酶(GAA)缺失而造成的是一种遗传性溶酶体贮积症。AT-GAA是第一款获得FDA突破性疗法认定的庞培病在研疗法。庞培病患者由于GAA的缺失,导致糖原在细胞中积累,从而引起患者出现多种神经肌肉症状。其中包括严重肌无力,而且症状会不断恶化。根据GAA缺失的程度,庞培病可以分为婴儿型和晚发型两大类,婴儿型庞培病患者心脏
2019-03-04 -
FDA批准六联儿童疫苗
日前,赛诺菲(Sanofi)和默沙东(MSD)联合宣布,FDA批准双方共同开发的“六合一”儿童疫苗Vaxelis上市。这款疫苗能够同时预防白喉、破伤风、百日咳、乙肝、脊髓灰质炎、和B型流感嗜血杆菌导致的侵袭性疾病。它适用于6周到4岁儿童。这款疫苗由默沙东和赛诺菲共同开发,赛诺菲将提供白喉、破伤风、百日咳和脊髓灰质炎的抗原,而默沙东将提供乙肝和B型流感嗜血杆菌的抗原。儿童需要在5周岁之前接受3次疫苗注射。这一疫苗已经在2016年在欧盟获得批准。这种“六合一”疫苗将减少儿童需要接受疫苗注射的次数,让
2019-01-03 -
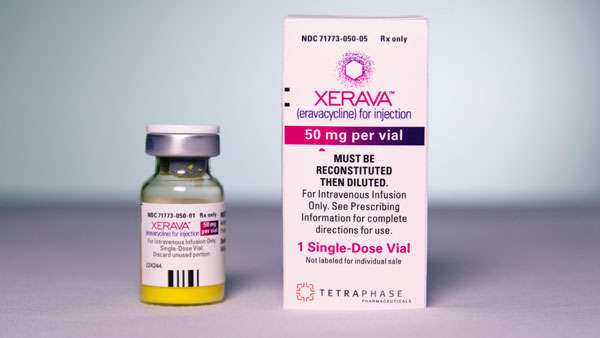
美国FDA批准 XERAVA(eravacycline)用于治疗复杂性腹腔内感染(cIAI)
今日,以治疗威胁生命的多重耐药(MDR)感染为目标,专注于开发和推广新型抗生素的生物医药公司Tetraphase Pharmaceuticals宣布,美国FDA批准 XERAVA™(eravacycline)用于治疗复杂性腹腔内感染(cIAI)。在临床试验中,eravacycline的耐受性良好,并且在cIAI患者中表现出高临床治愈率。它与两种广泛使用的抗生素——厄他培南和美罗培南相比,达到统计学非劣效性。腹腔内感染(IAI)是临床中的常见问题,包括多种疾病过程。根据感染程度,IAI被分为简单性
2018-08-29 -
诺华CAR-T细胞产品Kymriah两个适应症获欧盟批准
2018年8月27日,诺华公司宣布,欧盟委员会(EC)已经批准了Kymriah(tisagenlecleucel,曾名为CTL019)的两个适应症,分别为:▪ 用于治疗B细胞前体急性淋巴性白血病(ALL),且病情难治,或出现两次及以上复发的25岁以下患者▪ 用于治疗复发或难治性大B细胞淋巴瘤(r/r DLBCL)的成人患者(先前接受过两次或以上的系统治疗)值得注意的是,2017年8月30日,Kymriah已经成为了美国获批的第一个CAR-T细胞治疗产品,时隔一年,Kymriah再次成为了欧洲获批
2018-08-28 -
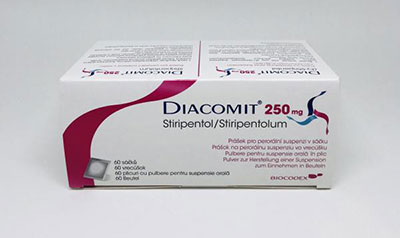
美国FDA批准儿童癫痫新药Diacomit(stiripentol)上市
日前,美国FDA宣布批准Biocodex公司研发的Diacomit(stiripentol)上市,与氯巴占(clobazam)联合使用,治疗2岁以上Dravet综合征患者的癫痫发作。值得一提的是,这也是美国FDA批准的第31款新药。Dravet综合征又称为婴儿严重肌阵挛性癫痫(Severe Myoclonic Epilepsy of infancy, SMEI)。它是一种罕见的难治性癫痫综合征,发病率约为1/15700。80%的患者在SCN1A基因上携带基因突变。患者的癫痫发病年龄早,在出生后第
2018-08-23 -
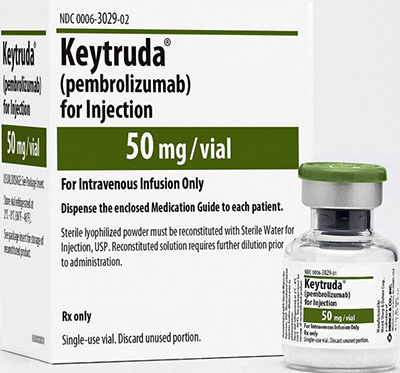
Keytruda获批标签扩展 联合Alimta及含铂化疗一线治疗NSCLC
默沙东近日宣布,美国食品和药物管理局(FDA)已批准PD-1免疫疗法Keytruda(pembrolizumab,帕博利珠单抗)的扩展标签,联合Alimta(pemetrexed,培美曲赛)及铂类化疗,用于无EGFR或ALK基因组肿瘤畸变的转移性非鳞状非小细胞肺癌(NSCLC)患者的一线治疗。此次批准是基于关键性III期临床研究KEYNOTE-189的数据。该研究由默沙东和礼来联合开展,这是一项随机、多中心、双盲、阳性对照研究,入组的患者为系统性疗法初治的转移性NSCLC患者,无论PD-L1肿瘤
2018-08-22 -
阿斯利康第三代靶向药Tagrisso(泰瑞沙)获日本批准
英国制药巨头阿斯利康(AstraZeneca)近日宣布,日本劳动卫生福利部(MHLW)已批准靶向抗癌药Tagrisso(osimertinib,奥西替尼)作为一种单药疗法,用于不能手术治愈的或复发性表皮生长因子受体(EGFR)突变阳性非小细胞肺癌(NSCLC)患者的一线治疗。此次批准是基于III期临床研究FLAURA的数据。这是一项随机、双盲研究,在556例(其中包括日本患者)既往未接受治疗(初治)的EGFR突变阳性(19号外显子删除或21号外显子L858R突变)局部晚期或转移性NSCLC患者中
2018-08-22 -
美国FDA批准Opdivo®新适应症用于经治小细胞肺癌
百时美施贵宝(NYSE:BMY)近日宣布,Opdivo®(nivolumab纳武利尤单抗)成为首个且唯一被美国FDA批准用于治疗既往接受过含铂方案化疗以及至少一种其他疗法1后疾病进展的转移性小细胞肺癌(SCLC)患者的免疫肿瘤(I-O)治疗药物。此次加速获批主要是基于总体应答率(ORR)和应答持续时间(DOR)的研究数据。该适应症的继续获批可能取决于在验证性试验中被证实和描述的临床获益1。百时美施贵宝胸部肿瘤开发部负责人Sabine Maier博士表示:“在百时美施贵宝,我们认识到为癌症患者提供
2018-08-22 -

罗氏靶向抗癌药Alecensa(艾乐替尼)获中国CNDA批准
瑞士制药巨头罗氏(Roche)近日宣布,中国国家药品监督管理局(CNDA)已批准Alecensa(alectinib,艾乐替尼),作为一种单药疗法,用于间变性淋巴瘤激酶(ALK)阳性晚期非小细胞肺癌(NSCLC)患者的治疗。值得一提的是,Alecensa通过优先审查获批,审批时间仅比欧洲药品管理局(EMA)和美国食品和药物管理局(FDA)一线批准晚了8个月和9个月。罗氏首席医疗官兼全球产品开发部负责人Sandra Horning表示,今天Alecensa获得CNDA批准,对中国ALK阳性肺癌患者
2018-08-21 -

FDA批准多动症新药JORNAY PM用于儿童的ADHD(注意力缺陷多动障碍)
HighlTherapeutics的全资子公司Ironshore,近日宣布FDA批准了其JORNAY PM(曾用名HLD200),用于治疗6岁以上儿童的ADHD(注意力缺陷多动障碍)。Jornay PM是一种新配方的哌甲酯,设计在晚间服用,用以改善第二天早起后严重的ADHD症状,其作用效果可延续一整天。Jornay PM是第一个使用Ironshore专有药物输送平台DELEXIS?的药物。Ironshore计划于2019年上半年启动Jornay PM的商业上市。ADHD是儿童期最常见的精神疾病,
2018-08-21 -
美国FDA加速批准首款特定白血病疗法
美国FDA宣布加速批准Blincyto(blinatumomab)的扩大适应症申请,允许这款由安进(Amgen)带来的新药治疗罹患B细胞前体急性淋巴性白血病(ALL),且在缓解期依旧有微小残留病灶(MRD)的儿童和成人患者。值得一提的是,这也是美国FDA批准的首款治疗MRD阳性ALL的疗法。B细胞前体ALL是一种病发于骨髓,且进展快速的癌症。患者的骨髓里会产生过多的不成熟白细胞,影响骨髓的功能。在这些患者经过治疗后,依旧会有不少人体内会带有微小残留病灶。尽管这些病灶在显微镜镜检下也无法被发现,但
2018-04-01 -
葛兰素史克带状疱疹疫苗Shingrix获欧盟和日本批准
英国制药巨头葛兰素史克(GSK)带状疱疹疫苗Shingrix近日在欧盟和日本监管方面同时传来喜讯。欧盟委员会(EC)已批准Shingrix,用于50岁及以上老年人群,预防带状疱疹(herpes zoster)及其并发症带状疱疹后神经痛(PHN);同时日本劳动卫生福利部(MHLW)批准Shingrix用于50岁及以上老年人群,预防带状疱疹。值得一提的是,Shingrix是首个横跨所有年龄组预防带状疱疹有效率≥90%的疫苗产品。Shingrix是一种非活、重组亚单位佐剂疫苗,通过2剂肌注(2针免疫程
2018-04-01

